Home > 纳米抗体能否提供更快速、更精确的靶向医疗?
经过 Jotbody
11 11 月, 2024
最新研究
纳米抗体能否提供更快速、更精确的靶向医疗?
在最近的一项突破性研究《Nanobodies Outperform Antibodies – Rapid Functionalization with Equal In Vivo Targeting Properties》中,研究人员展示了纳米抗体——一种紧凑的单域抗体——可替代传统抗体,提供同等的体内靶向能力,但具备更快速和高效的功能化过程。该发现解决了开发靶向疗法中的关键瓶颈:传统抗体尽管有效,但需要复杂且耗时的修饰才能在体内发挥功能,往往增加了成本和生产时间。

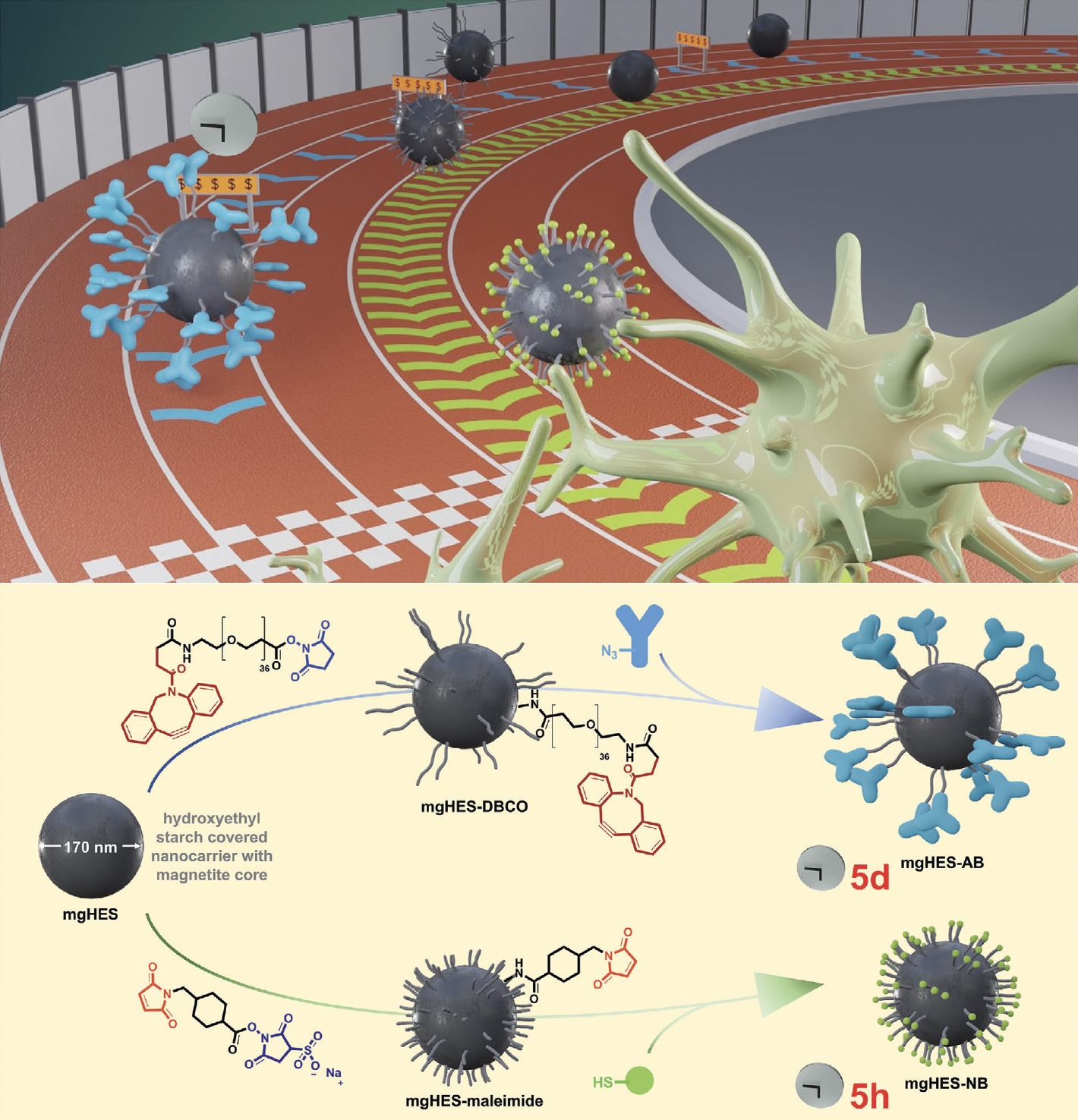
该研究的一大亮点是为纳米抗体添加了C末端半胱氨酸标签,使其能够通过硫醇-马来酰亚胺偶联技术轻松附着在纳米载体上。这一创新使得纳米抗体比传统抗体能够更快速、更精确地完成功能化或适用于医疗用途,同时在体内保持高特异性和稳定性。简化的偶联过程减少了所需的步骤和材料,使纳米抗体更易于生产且生产速度更快——这一优势对于在临床应用中实现规模化生产至关重要。

这种简化的过程意味着纳米抗体可以成为诊断和靶向药物递送中的宝贵工具,提供一种具成本效益的高精度解决方案,从而加速响应性医疗治疗的发展。本质上,该研究将纳米抗体突显为传统抗体的有力替代,具有通过更快捷、更高效的方式开发靶向治疗和诊断工具的潜力,从而推动精准医学的变革。
